Cómo convertir miligramos a miliequivalentes
Escrito por Estefanía Mac ; última actualización: March 29, 2019
La ciencia, en especial la química, puede ser un dolor de cabeza para los jóvenes en secundaria o en la universidad, en especial porque requiere que se desarrollen dos habilidades esenciales: pensamiento crítico y pensamiento abstracto.
Las fórmulas para realizar un cálculo de miliequivalentes a miligramos son realmente sencillas. Sin embargo, si no se comprenden las leyes de la química antes de hacerlo, se vuelve complicado.
Por eso el primer paso para emplear una fórmula de conversión de miligramos a miliequivalentes es entender algunos conceptos previos que ayudarán a que este método se perciba tan fácil como -realmente- lo es.
Te puede interesar: Cómo convertir mililitros a miligramos
Mg a mEq: ¿qué debes saber antes de comenzar a convertir?
Para empezar, es necesario descubrir el significado químico de la masa y del equivalente (EQ) químico, en ocasiones llamado peso equivalente, equivalente-gramo o simplemente, equivalente.
En ambos casos, se trata de una magnitud física que hace referencia a la cantidad de materia presente en un cuerpo. Mientras que la masa se mide en unidades de gramo o libras -y pudiera ser obtenida con el uso de una balanza- el equivalente es un constructo teórico definido como la masa requerida para obtener 1 mol de producto de reacción.
Esto aplica, sobre todo, en ácidos, bases y sales, y está definido matemáticamente en las siguientes fórmulas.
Fórmula del equivalente químico en ácidos

Cada uno de estos pesos se multiplica por la cantidad de átomos presente en el compuesto, así:Si se desea conocer, por ejemplo, el EQ del ácido fosfórico (H*3*PO*4*) en primer lugar, se calcula su peso molecular (P.M.). Para ello, se deben buscar los pesos atómicos (P.A.) de los átomos de hidrógeno (H), fósforo (P) y oxígeno (O) en una tabla periódica.
P.A. de H = 1
P.A. de P = 31
P.A. de O = 16
P.M. de H*3*PO*4* = (1 x 3) + (31 x 1) + (16 x 4) = 98 gramos / mol
Luego, se debe determinar la cantidad de hidrógeno presente en el ácido. En este caso, el ácido fosfórico presenta 3 átomos de hidrógeno.
Finalmente, se utiliza la ecuación de EQÁcido para saber el valor del equivalente químico:

Fórmula del equivalente químico en bases

De manera análoga, se puede conocer el equivalente químico de una base, como el hidróxido de hierro (III), Fe(OH)3.
En este caso, el peso molecular es de 107 g/mol y la cantidad de OH presente, 3.

Fórmula del equivalente químico en sales
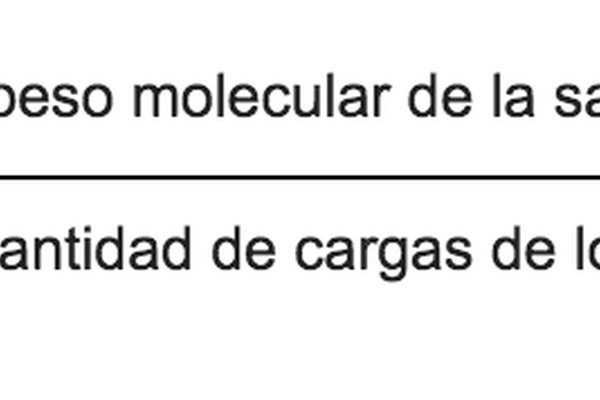
Para conocer la cantidad de cargas, lo único que debe hacerse es identificar los iones de la sal y sumar el valor neto de sus cargas. En el ejemplo, los iones son K+ y MnO4-, por lo que la cantidad de la carga neta existente es 2.Para las sales, igualmente se debe calcular el peso molecular. Por ejemplo, la sal permanganato de potasio, KMnO4 tiene un P.M. de 158 g/mol.

De cualquier forma, el primer paso para manejar las conversiones de mg a mEq y viceversa, es dominar el manejo de las ecuaciones trabajadas arriba. Una vez logrado eso, todo será más fácil.Ahora bien, en la mayoría de las reacciones químicas no se obtiene un mol de producto. Es decir, la reacción química se puede producir con cualquier cantidad de masa inicial, lo que permite obtener diversas cantidades de producto que pueden -o no- coincidir con el valor de 1 mol.
El secreto de mg a mEq es la regla de tres
La cuantificación de cualquier reacción química puede realizarse mediante un proceso básico: una regla de tres.
Los cálculos utilizados para determinar los valores de concentración, pureza de los compuestos químicos e incluso, los cambios de masa y volumen que se llevan a cabo durante una reacción química, se fundamentan en esa primera herramienta que se aprende en la escuela, conocida también como la regla de proporción o la regla de oro.
Regla de tres como fórmula para convertir miligramos a miliequivalentes
Veamos un caso práctico. El carbonato de litio (Li2CO3) es la sal metálica que le da el color rojo a los fuegos artificiales. La tonalidad aparece cuando la sal se calienta a altas temperaturas. Esto se da como consecuencia del proceso de excitación -y posterior retorno al estado basal- que sufren los átomos de litio en esas condiciones.
Para preparar los fuegos artificiales, se efectúan mezclas que consisten -principalmente- en pólvora y sales, como el carbonato de litio. En estos casos, los especialistas prefieren realizar los cálculos en base a los equivalentes, en lugar de gramos o miligramos.
Para ello, obtienen el equivalente químico, tal como se mostró en el apartado anterior de fórmulas, lo que da como resultado lo siguiente:
- El peso molecular del Li2CO3 es de 74 g/mol
- La cantidad de carga total es 4 (dos iones de litio y un ión de carbono que vale por dos cargas)
- Por ende, su equivalente (EQ) es 18,5, que es el resultado de dividir 74 entre 4
Observación: un mol de Li2CO3 tiene una masa de 74 g
Podría interesarte: Valoración del carbonato de sodio con ácido clorhídrico
Ejemplo de mg a mEq:
En la industria farmacéutica y en el sector de la salud, se suele trabajar con cantidades muy pequeñas, cercanas a una centésima o milésima de gramo. Por ello, es preferible hacer uso de los términos miligramos (mg) y miliequivalentes (mEq).
Considera que 1 gramo es igual 1.000 mg y 1 equivalente es igual a 1 gramo. Basándonos en esta información:
74 g de Li2CO3 = 74.000 mg de Li*2*CO3
18 EQ de Li2CO3 = 18.000 EQ de Li*2*CO3
Veámoslo en un ejemplo. Supongamos que queremos convertir 800 mg de Li*2*CO*3* en miliequivalentes (mEq), conociendo que el equivalente de este compuesto es 18,5 EQ, tal como descubrimos en el ejemplo anterior.
En este caso, se puede realizar la conversión mediante una sencilla de regla de tres:
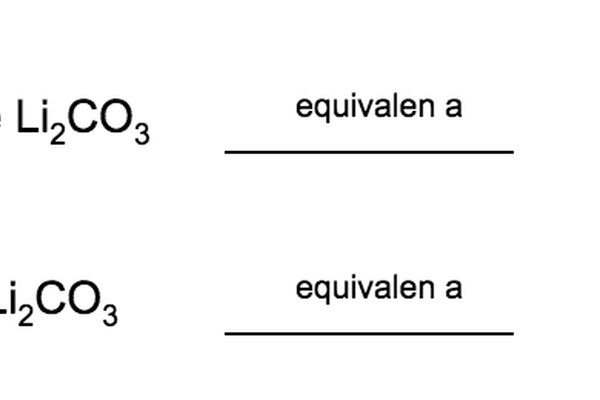
0,2 EQ x 1.000 = 200 mEqLa resolución de la presente regla de tres arroja que X es igual a 0,2 EQ. Lo único que hay que hacer ahora es multiplicar este dato por 1.000, ya que 1 equivalente es igual a 1.000 miliequivalentes:
En conclusión:
- Para convertir miligramos a miliequivalentes se debe conocer primero el peso molecular de la sal, ácido o base, usualmente expresado en gramos/mol
- Después, hay que calcular el equivalente del compuesto con las fórmulas indicadas
- Si ya se tiene el peso molecular en miligramos y el equivalente, basta con hacer una regla de tres
- El resultado de la regla de tres se multiplica por 1.000 para conseguir la cifra expresada en miliequivalentes
Más artículos
Cómo calcular la alcalinidad de CaCO3→

Cómo convertir miligramos a mEq Cr→

Cómo encontrar el estado de oxidación y carga iónica de un elemento→

Cómo convertir mEq en ppm→

Cómo convertir microgramos y mililitros a milimoles→

Cómo encontrar el CV y CP teniendo en cuenta una proporción en química física →
