Cómo determinar la carga de iones basándote en la tabla periódica
Escrito por Lee Johnson ; última actualización: February 01, 2018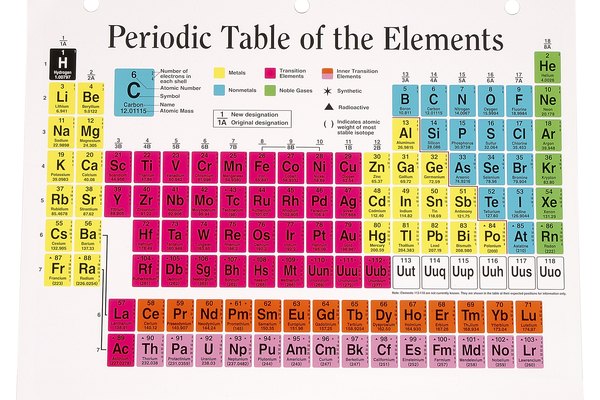
Si estás estudiando los enlaces iónicos y quieres saber qué iones se unen entre sí, puedes aprender a determinar las cargas de iones basándote en la tabla periódica. Los enlaces iónicos ocurren cuando los elementos forman iones al ganar o perder electrones y, por lo tanto, desarrollan cargas magnéticas. Las cargas opuestas se atraen y, de esta manera, forman enlaces entre iones. Se pueden determinar las cargas de la mayor parte de los iones a partir de la ubicación de los elementos en la tabla periódica, pero algunos grupos de elementos no pueden clasificarse de este modo con facilidad.
Busca una tabla periódica (observa las fuentes). La mayoría de las tablas ubican los números de grupo en la fila superior. Los grupos son columnas que van de izquierda a derecha secuencialmente. Ten en cuenta que el hidrógeno y el litio están en el grupo uno y el helio y el neón en el grupo 18. Busca una tabla periódica que incluya las cargas iónicas para facilitar el proceso. Encuentra el número al lado del "+" o el “-” en la parte superior derecha del símbolo del elemento para encontrar la carga.
Ten en cuenta que los grupos uno, dos y tres (las tres columnas ubicadas en el extremo más izquierdo) tienen cargas iónicas positivas relacionadas a su número de grupo. Los elementos del grupo uno tienen una carga “1+” y los del grupo dos una carga “2+”. Asimismo, los elementos del grupo tres tienen una carga “3+”.
Utiliza los números romanos al lado de elementos como el titanio y el hierro. El titanio, en la parte superior del grupo cuatro, está seguido ya sea de “(IV)” o “(III)", que indican la carga del ion. El titanio puede adaptarse a otros elementos de este grupo y tener una carga iónica de “4+”. Ten en cuenta que los elementos del grupo cinco son similares, con el vanadio y el niobio siendo capaces de formar iones “3+” y “5+". El tantalio siempre tiene una carga de “5+”. Los grupos seis y siete también tienen cargas correspondientes (“6+” y “7+”) a menos que los números romanos indiquen lo contrario.
Recuerda que el osmio y el iridio tienen cargas “4+” y el rodio tiene una carga “3+”. Los grupos ocho y nueve no pueden clasificarse con tanta facilidad como los grupos previos, pero afortunadamente sólo estos tres elementos no incluyen los números romanos. Todos los elementos del grupo 10 tienen números romanos para indicar la carga iónica.
Considera los elementos del grupo 11, 12, 13, 14 y 15 como similares a los grupos del uno al cinco. La carga de todos los elementos del grupo 11 (además de aquellas indicadas por los números romanos) es “1+" y todos los elementos del grupo 12 pueden tener una carga de “2+". Esto continúa con los metales de los grupos 13 al 15, en los que todos los elementos pueden hacer la carga relevante (si restas 10 al número de grupo) y otros están indicados por los números romanos. La carga de los metales del grupo 16 sólo puede estar determinada por los números romanos.
Aprende las cargas negativas de los no metales de los grupos. Todos los no metales del grupo 15 forman iones con cargas “3-” y los no metales del grupo 16 forman iones con cargas “2-”. Todos los elementos del grupo 17 tienen iones “1-”. Recuerda que los gases nobles del grupo 18 tienen capas de electrones completas y, por lo tanto, no forman iones.
Recuerda que los lantánidos y actínidos no forman una carga “3+” y no están expresados en números romanos. El torio forma un ion “4+” y el neptunio un ion “5+”. El resto de los lantánidos y actínidos tienen números romanos para indicar la carga o tienen cargas “3+”.
Más artículos
Cómo usar la regla del octeto→

Cómo encontrar el estado de oxidación y carga iónica de un elemento→

Cómo calcular la valencia→

¿Cómo encontrar el número de iones en un elemento?→
Cómo saber el número de electrones de valencia al escribir configuraciones electrónicas→

Cómo obtener el número total de valencias en un compuesto →
