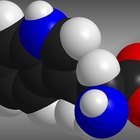
¿Qué es un hidrato en Química?
Escrito por Angela Libal ; última actualización: February 01, 2018
Hay una serie de fenómenos que ocurren naturalmente en el mundo que nos rodea, pero que nuestra ciencia recién ahora está empezando a comprender. Una ocurrencia tal es la formación del hidrato, un compuesto químico creado con un número de moléculas diferentes y un denominador común: el agua.
Definición
Un hidrato es una molécula que contiene un cierto tipo de agua. A menudo, una molécula base se toma y una molécula de agua se añade a la misma, con el fin de crear otra molécula con propiedades diferentes. En algunos casos, las moléculas de agua se convierten en una parte de la estructura de la molécula original. En otros casos el agua está unida al centro de la molécula, en lugar de mezclarse en la estructura. Este proceso se denomina agua de hidratación. Por ejemplo, el hidrato de cloral (como se ve en la ilustración) es el hidrato de una molécula de cloral. El cloral reacciona con el agua para formar una sustancia totalmente diferente, el hidrato de cloral, que es uno de los ingredientes fundamentales en el pesticida DDT y actúa como un sedante.
Historia
La investigación sobre las propiedades y usos de los hidratos comenzó a principios de 1800 como parte de una investigación llevada a cabo por Humphry Davy y Michael Faraday. Mientras se experimentaba con mezclas de cloro y agua, los científicos se dieron cuenta de que habían extrañas formaciones que se cristalizaban en las muestras cuando se encontraban muy por encima del punto de congelación del agua. Ellos desarrollaron la teoría de que las moléculas se estaban estabilizando por la unión con otra molécula más estable en las inmediaciones. No fue sino hasta la década de 1930 que otro científico, EG Hammerschmidt, determinó que estas rarezas eran responsables de causar obstrucciones en las líneas de gas natural que atravesaban las zonas frías. Por la década de 1970, las condiciones para la formación de metano habían sido aisladas. Se pensó que el hidrato de metano sería una forma natural de energía de gas. Los esfuerzos de Rusia produjeron hidratos de metano de las profundidades del océano, fomentando la investigación para dar un paso más en la creación y aplicación de los hidratos como fuente de energía natural.
Función
Los hidratos cambian la molécula base de los enlaces de agua mismos, y el resultado es un compuesto que es tan flexible como numeroso. Los hidratos diferentes tienen usos distintos, y algunos se utilizan todos los días. Se encuentran comúnmente en productos para el cuidado de la piel tales como el bálsamo hidratante, el champú y las cremas para labios. Los hidratos le regresan la humedad a la piel y reparan el tejido dañado por el frío y la sequedad. Se utilizan en muchos procesos industriales, especialmente cuando dos compuestos necesitan ser separados. Un ejemplo de esto es la desalación, o la extracción de la sal del agua. El hidrato se combina con el agua salada en bruto, y los enlaces dentro cambian las moléculas. Hay algunas moléculas que son más fácilmente combinadas que otras, y mediante el uso de este principio es posible crear agua dulce de agua salada. El mismo principio también funciona con los gases.
Consideraciones
Es posible para un hidrato perder su molécula de agua, cuando esto ocurre, se denomina un anhídrido. Por ejemplo, el hidróxido de sodio es un compuesto que es comúnmente conocido como lejía. En este sentido, su forma hidratada, es un ingrediente común en los jabones, detergentes y limpiadores de desagües. La lejía es un producto químico tóxico de uso frecuente en su forma cruda como agente de descomposición que se utiliza con los cadáveres de animales de granja y muertes en las vías. Con el agua removida del compuesto químico, sin embargo, el hidrato se convierte en el óxido de sodio anhídrido. Éste es uno de los componentes críticos en la fabricación de vidrio.
Potencial
El potencial de estos hidratos de origen natural ha intrigado a los científicos durante décadas, especialmente los hidratos de metano. En esta combinación, la molécula de agua rodea completamente la molécula de metano sin llegar a unirse a ella. Se piensa por la comunidad científica, que existe una posibilidad de aprovechar la energía almacenada en el hidrato de metano para una futura fuente de energía. Bajo las condiciones adecuadas, la investigación ha encontrado que en el fondo del mar hay varios hidratos de metano que pueden ser producidos económicamente y en cantidades masivas. Sin embargo, hay una serie de cuestiones que hay que superar en primer lugar, incluidas las prácticas de perforación seguras y la estabilidad del medio ambiente en el que se encuentra el hidrato.
Más artículos
Los efectos dañinos del Reino Monera→
Similitudes entre los ecosistemas marinos y los de agua dulce→

Maneras científicas de separar el petroleo del agua→

¿Cuáles son los agentes de meteorización?→

¿Cuál es la diferencia entre el etanol y el alcohol?→

Por qué el carbono es tan importante para los compuestos orgánicos→